
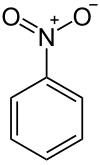
硝基苯
硝基苯
Подписчиков: 0, рейтинг: 0
| 硝基苯 | |||
|---|---|---|---|
| |||
|
| |||

| |||
| 英文名 | Nitrobenzene | ||
| 识别 | |||
| CAS号 |
98-95-3 |
||
| PubChem | 7416 | ||
| ChemSpider | 7138 | ||
| SMILES |
|
||
| InChI |
|
||
| InChIKey | LQNUZADURLCDLV-UHFFFAOYAA | ||
| ChEBI | 27798 | ||
| RTECS | QJ0525000 | ||
| KEGG | C06813 | ||
| 性质 | |||
| 化学式 | C6H5NO2 | ||
| 摩尔质量 | 123.06 g·mol⁻¹ | ||
| 外观 | 黄色油状液体 | ||
| 氣味 | 像鞋油那样刺鼻 | ||
| 密度 | 1.20 g/cm3(20 °C) | ||
| 熔点 | 6 °C | ||
| 沸点 | 211 °C | ||
| 溶解性(水) | 0.19 g/100 ml(20 °C) | ||
| 溶解性 | 与乙醇、乙醚和苯混溶 | ||
| 蒸氣壓 | 0.3 mmHg (25°C) | ||
| 磁化率 | -61.80·10−6 cm3/mol | ||
| 黏度 | 1.8112 mPa·s | ||
| 危险性 | |||
GHS危险性符号 
| |||
| GHS提示词 | Danger | ||
| H-术语 | H301, H311, H331, H351, H360, H372, H412 | ||
| P-术语 | P201, P202, P260, P261, P264, P270, P271, P273, P280, P281, P301+310, P302+352, P304+340, P308+313 | ||
| NFPA 704 | |||
| 闪点 | 88 °C | ||
| 爆炸極限 | 1.8%-? | ||
| PEL | TWA 1 ppm (5 mg/m3) [皮肤] | ||
| 致死量或浓度: | |||
|
LD50(中位剂量)
|
780 mg/kg(大鼠,口服) 600 mg/kg(大鼠,口服) 590 mg/kg(小鼠,口服) |
||
|
LDLo(最低)
|
750 mg/kg(狗,口服) | ||
| 相关物质 | |||
| 相关化学品 |
苯胺 苯基重氮盐 亚硝基苯 |
||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
硝基苯是最简单的芳香硝基化合物,化学式为C6H5NO2。它是由米修里希·伊尔哈得于1834年发现的。
生产
硝基苯可以由苯被硝酸和浓硫酸的混合物硝化而成。反应首先会形成硝𬭩离子,然后硝𬭩离子和苯反应生成硝基苯:
由于反应高度放热(ΔH = −117 kJ/mol),硝基苯的生产是工业上最危险的生产流程之一。
硝基苯在1985年的年产量约为 1,700,000 吨。
应用
生产出来的硝基苯有95%都会被氢化成苯胺,而苯胺是聚氨酯、橡胶化学品、除草剂、染料和药物的前体。
- C6H5NO2 + 3 H2 → C6H5NH2 + 2 H2O
硝基苯还用于掩盖鞋和地板抛光剂、皮革敷料、油漆溶剂和其它材料中的难闻气味。在之前,硝基苯还用于曾被用来使肥皂更香,但今天已经被毒性更低的化合物淘汰了。硝基苯还可以生产镇痛剂扑热息痛。由于不寻常高的克尔常数,硝基苯也用于制造克尔盒。有证据表明硝基苯可以在农业中用作植物生长和开花的刺激剂。
有机合成
除了氢化成苯胺外,硝基苯还可以被还原成氧化偶氮苯、偶氮苯、亚硝基苯、二苯肼和苯基羟胺。在斯克劳普合成反应中,硝基苯也用作温和的氧化剂。
危害
长期暴露于硝基苯下会对中枢神经系统造成严重影响,还会损害视力、导致肝或肾损伤、贫血和刺激肺部。吸入蒸气可能会导致头痛、恶心、疲劳、头晕、紫绀、手臂和腿部虚弱,在极少数情况下可能是致命的。硝基苯很容易通过皮肤吸收,可能会增加心率,导致抽搐。摄入硝基苯同样会引起头痛、头晕、恶心、呕吐和胃肠道刺激、四肢失去知觉无法控制,还会导致内出血。
硝基苯很可能是致癌物,并被国际癌症研究机构归类为2B类致癌物(可能对人类致癌)。它已被证明会导致大鼠的肝脏、肾脏和甲状腺得癌。
硝基苯中毒可以用抗坏血酸(中毒较轻)或甲苯胺蓝(中毒较重)解毒。使用甲苯胺蓝解毒时,患者的皮肤会暂时变蓝。对于可以危及生命的中毒则需要换血。
参考资料
外部链接
- International Chemical Safety Card 0065 (页面存档备份,存于互联网档案馆)
- NIOSH Pocket Guide to Chemical Hazards (页面存档备份,存于互联网档案馆)
- IARC Monograph: "Nitrobenzene" (页面存档备份,存于互联网档案馆)
- US EPA factsheet (页面存档备份,存于互联网档案馆)
- https://patents.google.com/patent/US9113628 (页面存档备份,存于互联网档案馆)
| |||||||||||||||||||||||||||||||||||||
|




