G蛋白偶联受体
| GPCR | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
| 鑑定 | |||||||||
| 標誌 | 7tm_1 | ||||||||
| Pfam | PF00001(旧版) | ||||||||
| InterPro | IPR000276 | ||||||||
| PROSITE | PDOC00210 | ||||||||
| OPM家族 | 6 | ||||||||
| OPM蛋白 | 1gzm | ||||||||
| |||||||||
G蛋白偶联受体(G protein-coupled receptor,GPCRs),是一大类膜蛋白受体的统称。
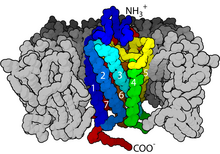
这类受体的共同点是其立体结构中都有七个跨膜α螺旋,且其肽链的C端和连接第5和第6个跨膜螺旋的胞内环上都有G蛋白(鸟苷酸结合蛋白)的结合位点。
目前为止,只在真核生物中发现G蛋白偶联受体。它们参与很多细胞信号转导过程。在这些过程中,G蛋白偶联受体能结合细胞周围环境中的化学物质并激活细胞内的一系列信号通路,最终引起细胞状态的改变。已知的与G蛋白偶联受体结合的配体包括气味分子、费洛蒙、荷尔蒙、神经递质、趋化因子等等。这些受体可以是小分子的糖类、脂质、多肽,也可以是蛋白质等生物大分子。一些特殊的G蛋白偶联受体也可以被非化学性的刺激源激活,例如在感光细胞中的视紫红质可以被光所激活。与G蛋白偶联受体相关的疾病为数众多,并且大约40%的现代药物都以G蛋白偶联受体作为靶点。
G蛋白偶联受体的下游信号通路有多种。与配体结合的G蛋白偶联受体会发生构象变化,从而表现出鸟苷酸交换因子(GEF)的特性,通过以三磷酸鸟苷(GTP)交换G蛋白上本来结合着的二磷酸鳥苷(GDP)使G蛋白的α亚基与β、γ亚基分离。这一过程使得G蛋白(特别地,指其与GTP结合着的α亚基)变为激活状态,并参与下一步的信号传递过程。具体的传递通路取决于α亚基的种类(Gαs、Gαi/o、Gαq/11、Gα12/13)。其中主要的两个通路分别以由三磷酸腺苷环化产生的环腺苷酸(cAMP)和由磷脂酰肌醇-4,5-二磷酸(PIP2)水解生成的肌醇三磷酸(IP3)和甘油二酯(DAG)作为第二信使, 详见环腺苷酸信号通路和磷脂酰肌醇信号通路。
目录
历史和意义
2012年的诺贝尔化学奖颁发给了布赖恩·科比尔卡和罗伯特·莱夫科维茨,以表彰他们对于G蛋白偶联受体的功能的研究。对于G蛋白介导的信号传导的某些方面,至少获得另外七项诺贝尔奖 。2012年全球销量最高的十种药物中的两种(Advair Diskus和Abilify)即属此类 。
分类
G蛋白偶联受体组成了一个非常庞大的蛋白质超家族(protein superfamily)。这个超家族的具体大小尚未知晓,不过依据DNA序列的相似性,人们预测人类基因组中有约800个基因(约占整个基因组中编码蛋白质的部分的4%)会编码G蛋白偶联受体超家族的成员蛋白。 这些G蛋白偶联受体可以被大致划分为六个类型,分属其中的G蛋白偶联受体的基因序列之间没有显著的同源关系。
- A 类(或 第一类)(视紫红质样受体)
- B 类(或 第二类)(分泌素受体家族)
- C 类(或 第三类)(代谢型谷氨酸受体/信息素)
- D 类(或 第四类)(真菌交配信息素受体)
- E 类(或 第五类)(环腺苷酸受体)
- F 类(或 第六类)(卷曲受体(Frizzled)/Smoothened家族)
其中第一类即视紫红质样受体包含了绝大多数种类的G蛋白偶联受体。它被进一步分为了19个子类A1-A19。最近,有人提出了一种新的关于G蛋白偶联受体的分类系统,被称为GRAFS,即谷氨酸(Glutamate),视紫红质(Rhodopsin),粘附(Adhesion),Frizzled/Taste2以及分泌素(Secretin)的英文首字母缩写。
一些基于生物信息学的研究着眼于预测那些具体功能尚未明了的G蛋白偶联受体的分类。研究者使用被称为伪氨基酸组成的方法利用G蛋白偶联受体的氨基酸系列来预测它们在生物体内可能的功能以及分类。
受体结构
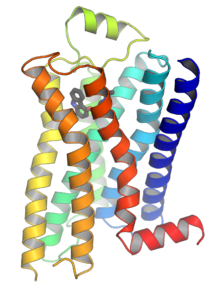
G蛋白偶联受体均是膜内在蛋白(Integral membrane protein),每个受体内包含七个α螺旋组成的跨膜结构域,这些结构域将受体分割为膜外N端(N-terminus),膜内C端(C-terminus),3个膜外环(Loop)和3个膜内环。受体的膜外部分经常带有糖基化修饰。膜外环上包含有两个高度保守的半胱氨酸残基,它们可以通过形成二硫键稳定受体的空间结构。有些光敏感通道蛋白(Channelrhodopsin)和G蛋白偶联受体有着相似的结构,也包含有七个跨膜螺旋,但同时也包含有一个跨膜的通道可供离子通过。
与G蛋白偶联受体相似,两种脂联素受体(ADIPOR1和ADIPOR2)也包含七个跨膜域,但是它们以相反的方向跨于膜上(即N端在膜内而C端在膜外),并且它们也不与G蛋白相互作用。
早期关于G蛋白偶联受体结构的模型是基于他们与细菌视紫红质(Bacteriorhodopsin)之间微弱的趋同演化关系的,其中后者的结构已由电子衍射(蛋白质数据库资料编号:PDB 2BRD和PDB 1AT9)和X射线晶体衍射(PDB 1AP9)实验所获得。在2000年,第一个哺乳动物G蛋白偶联受体——牛视紫红质的晶体结构(PDB 1F88)被解出。 2007年,第一个人类G蛋白偶联受体的结构(PDB 2R4R和PDB 2R4S)被解出。随后不久,同一个受体的更高解析度的结构(PDB 2RH1)被发表出来。这个人G蛋白偶联受体——β2肾上腺素能受体,显示出与牛视紫红质的高度相似,不过两者在第二个膜外环的构象上完全不同。由于第二膜外环组成了一个类似盖子的结构罩住了配体结合位点,这个构象上的区别使得所有对从视紫红质建立G蛋白偶联受体同源结构模型的努力变得困难重重。
一些激活的即结合了配体的G蛋白偶联受体的结构也已经被研究清楚。这些结构显示了G蛋白偶联受体的膜外部分与配体结合了之后会导致膜内部分发生构象变化。其中最显著的变化是第五和第六跨膜螺旋之间的膜内环会向外移动,而激活的β2肾上腺素能受体与G蛋白形成的复合体的结构显示了G蛋白α亚基正是结合在了上述运动所产生的一个空穴处。
生理作用
G蛋白偶联受体参与众多生理过程。包括但不限于以下例子:
- 感光:视紫红质是一大类可以感光的G蛋白偶联受体。它们可以将电磁辐射信号转化成细胞内的化学信号,引导这一过程的反应称为光致异构化(Photoisomerization)。具体细节为:由视蛋白(Opsin)和辅因子视黄醛共价连接所构成的视紫红质在光源的刺激下,分子内的视黄醛会发生异构化,从“11-顺式”变成“全反式”,这个变化进一步引起视蛋白的构象变化从而激活与之偶联的G蛋白,引发下游的信号传递过程。
- 味觉感觉(味道):味细胞中的GPCR响应苦味和甜味物质介导味觉素(Gustducin)的释放。
- 嗅觉:鼻腔内的嗅上皮(Olfactory epithelium)和犁鼻器上分布有很多嗅觉受体,可以感知气味分子和费洛蒙。
- 行为和情绪的调节:哺乳动物的脑内有很多掌控行为和情绪的神经递质对应的受体是G蛋白偶联受体,包括血清素,多巴胺,γ-氨基丁酸和谷氨酸等。
- 免疫系统的调节:很多趋化因子通过G蛋白偶联受体发挥作用,这些受体被统称为趋化因子受体。其它属于此类的G蛋白偶联受体包括白介素受体(Interleukin receptor)和参与炎症与过敏反应的组胺受体(Histamine receptor)等。
- 自主神经系统的调节:在脊椎动物中,交感神经和副交感神经的活动都受到G蛋白偶联受体信号通路的调节,它们控制着很多自律的生理功能,包括血压,心跳,消化等。
- 细胞密度的调节:最近在盘基网柄菌中发现了一种含有脂质激酶活性的G蛋白偶联受体,可以调控该种黏菌对细胞密度的感应。
- 维持稳态:例如机体内水平衡的调节。
- 参与某些类型肿瘤的生长和遠端轉移。
机理
G蛋白偶联受体传递信号的机理包括几个主要步骤:首先来自细胞膜外侧的配体与受体相结合,引起后者的构象变化,这个过程也称为受体的激活。发生了构象变化的受体随即会激活附着在其细胞膜内侧端的G蛋白,表现为G蛋白上原先结合的GDP被替换为GTP。激活后的G蛋白会进一步引发一系列的下游效应,其中所涉及的具体信号通路则取决于G蛋白的种类。
配体结合位点
大部分A类受体的配体结合部位处于跨膜螺旋和胞外环附近,不过也有一些例外,如糖蛋白激素受体(GPHR)和富亮氨酸重复G蛋白偶联受体(LGR)等。其它类型的G蛋白偶联受体则主要以N端与配体结合。 也有一些报道指出B类受体的跨膜螺旋上也存在潜在的变构配体结合位点。
构象变化
在静息状态下,G蛋白偶联受体在膜上与由Gα、Gβ和Gγ三个亚基组成的异三聚体G蛋白结合形成复合物。其中Gα亚基上结合有GDP分子。当有配体结合到受体上时会引起后者的构象发生变化,变成具有鸟苷酸交换因子活性的“活化构象”。活化的受体会催化Gα亚基捕获GTP分子来交换其上结合着的GDP。GTP与Gα亚基的结合会使受体与G蛋白的复合物解离,受体、GTP-Gα和Gβ-Gγ二聚体三者相互分开。其中后两者可以进一步与其它蛋白相互作用从而使信号继续传递下去,而自由的受体可以重新结合上一个新的G蛋白来开始下一轮信号转导过程。
配体
除了部分情况下可由可见光激活外,生理条件下正常工作的G蛋白偶联受体主要由配体分子所激活。可以与G蛋白偶联受体结合的配体涵盖了很多种类的信号分子,包括各种气味分子、腺苷、肝细胞生长因子(HGF)、一些生物胺(如多巴胺、肾上腺素、去甲肾上腺素、组胺和血清素等)、谷氨酸(通过代谢型谷氨酸受体)、胰高血糖素、乙酰胆碱(通过毒蕈碱型乙酰胆碱受体)、大麻素、趋化因子、介导炎症反应的一些脂质(如前列腺素等类花生酸、血小板活化因子和白三烯等)以及众多肽类激素(如降钙素、生长抑素、生长激素、部分血管活性肠肽家族的成员、抗利尿激素、过敏毒素、促卵泡激素、促性腺激素释放激素、速激肽、缓激肽、蛙皮素、内皮素、γ-氨基丁酸、黑素皮质激素、神经肽Y、阿片肽、促甲状腺素释放激素和催产素等)。另外,也有些G蛋白偶联受体虽然与其它已确认的受体结构上明显相似,但是其內源配体尚未被发现,这样的G蛋白偶联受体同其它类似的受体一起被归类为孤儿受体。
第二信使系统
环腺苷酸信号通路
磷脂酰肌醇信号通路
下游信号通路
调控机理
蛋白激酶A介导的磷酸化
G蛋白偶联受体激酶介导的磷酸化
信号终止机制
寡聚化
G蛋白偶联受体超家族的起源与演化
参见
参考资料
外部链接
| 维基共享资源中相关的多媒体资源:G蛋白偶联受体 |
- 醫學主題詞表(MeSH):G-protein-coupled+receptors
- (英文)GPCR Cell Line
- (英文)GPCR Database. IUPHAR Database. International Union of Basic and Clinical Pharmacology. [11 August 2008]. (原始内容存档于2012-03-20).
-
(英文)GPCRdb. [2018-03-31]. (原始内容存档于2020-10-27).
Data, diagrams and web tools for G protein-coupled receptors (GPCRs).
; Munk C, Isberg V, Mordalski S, Harpsøe K, Rataj K, Hauser AS, Kolb P, Bojarski AJ, Vriend G, Gloriam DE. GPCRdb: the G Protein-Coupled Receptor Database – an Introduction. British Journal of Pharmacology. 2016, 173 (14): 2195–207. PMC 4919580 . PMID 27155948. doi:10.1111/bph.13509.
. PMID 27155948. doi:10.1111/bph.13509.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||