
高锰酸钾
| 高锰酸钾 | |
|---|---|
| |

| |
|
IUPAC名 Potassium permanganate | |
| 别名 | 灰锰氧、PP粉 |
| 识别 | |
| CAS号 |
7722-64-7 |
| PubChem | 516875 |
| ChemSpider | 22810 |
| SMILES |
|
| UN编号 | 1490 |
| EINECS | 231-760-3 |
| RTECS | SD6475000 |
| KEGG | D02053 |
| 性质 | |
| 化学式 | KMnO₄ |
| 摩尔质量 | 158.04 g·mol⁻¹ |
| 外观 | 紫黑色针状结晶 |
| 密度 | 2.703 g/cm³ |
| 熔点 | 240℃分解 |
| 溶解性(水) | 6.51 g/100 ml,20℃ 32.35 g/100 ml,75℃ |
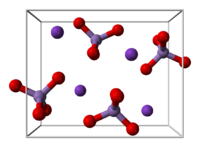
| 结构 | |
| 晶体结构 | 正交晶系 |
| 热力学 | |
| ΔfHm⦵298K | −813.4 kJ·mol−1 |
| S⦵298K | 171.7 J·K−1·mol−1 |
| 危险性 | |
|
欧盟危险性符号 | |
| 警示术语 | R:R8-R22-R51/53 |
| 安全术语 | S:S2-S60-S61 |
| MSDS | 英文MSDS |
| NFPA 704 | |
| 相关物质 | |
| 其他阴离子 |
高锝酸钾 高铼酸钾 |
| 其他阳离子 |
高锰酸钠 高锰酸铵 高锰酸鈣 |
| 相关化学品 |
锰酸钾 七氧化二锰 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
高锰酸钾(英語:Potassium permanganate;化学式KMnO₄),强氧化剂,紫黑色晶体,可溶于水,遇乙醇即还原。常用作消毒剂、水净化剂、氧化剂、漂白剂、毒气吸收剂、二氧化碳精制剂等。1659年由约翰·格劳勃發現。在醫療用作清潔消毒和消滅真菌。
目录
来源
實驗室對其需求高,高錳酸鉀的製造規模大。一般常見製備方法有以下兩種:
礦石中取得的二氧化錳和氢氧化钾在空氣中或混合硝酸鉀(提供氧氣)加熱,產生錳酸鉀,再於鹼溶液與氧化劑電解氧化得到過錳酸鉀。
- 2MnO₂+4OH⁻+O₂ → 2MnO₄²⁻+2H₂O
- 2 MnO₄²⁻+Cl₂ → 2MnO₄⁻+2Cl⁻
或者也可以二氧化鉛或鉍酸鈉等強氧化劑氧化Mn²⁺生成。過錳酸鉀的顏色明顯,此反應也用於檢驗Mn²⁺。
化學性质
对热不稳定
这是实验室制取氧气的方法之一。加热时如果温度更高,生成的锰酸钾则可以继续分解。
也有文献指出,高锰酸钾的分解过程不会产生二氧化锰,而只有K₂MnO₄、K₂Mn₄O8和KMnO₂:
另有实验得出不同的分解历程:
强氧化力
高锰酸钾有强氧化力,可以在常温氧化盐酸,这也是实验室制取氯气的方法之一:
2KMnO₄+16HCl → 2KCl+2MnCl₂+5Cl₂↑+8H₂O
高锰酸钾也可用亚硫酸钠还原,得到不稳定的亮蓝色的五价锰盐(MnO₄³⁻),極易再被亞硫酸鈉還原產生更低價的錳化合物。
高锰酸钾与过氧化氢会剧烈反应,生成氧气;在酸中则会生成锰盐:
2KMnO₄+3H₂O₂ → 2KOH+2MnO₂+2H₂O+3O₂↑
2KMnO₄+5H₂O₂+6H⁺ → 2K⁺+2Mn²⁺+8H₂O+5O₂↑
高锰酸钾氧化Mn²⁺生成MnO₂沉淀。但有焦磷酸存在时,则按下式反应:
- 4Mn²⁺+MnO₄⁻+8H⁺+15H₂P₂O7²⁻ → 5[Mn(H₂P₂O7)₃]³⁻+4H₂O
利用其氧化性的特点,可用有还原力的草酸、维生素C或盐酸羟胺等溶液去除高锰酸钾造成的污渍。
另外,高锰酸钾可以和红磷、镁粉、铝粉、硼氢化钠等还原剂形成易爆混合物,摩擦或撞击即可爆炸;不應混合在一起。
其他
- 6KMnO₄+4Al₂(SO₄)₃·18H₂O+6H₂O → 2Al(MnO₄)₃+6KAl(SO₄)₂·12H₂O
過錳酸根的還原產物因pH而異:強鹼中生成墨綠色的錳酸根MnO₄²⁻,在中性和弱鹼中生成棕黑色的MnO₂水合物,而在強酸中則生成極淺粉紅色Mn²⁺。
安全
高锰酸钾是强氧化剂,应与可氧化的物质隔开存放。高锰酸钾与浓硫酸反应生成易爆物七氧化二锰。固体高锰酸钾与纯甘油或一些醇反应会剧烈燃烧。
- 3C₃H₅(OH)₃+14KMnO₄ → 14MnO₂+7K₂CO₃+2CO₂↑+12H₂O
常温可和甘油等有机物反应甚至燃烧(但有时与甘油混合后反应极为缓慢,甚至感受不到温度升高,原因尚不明确);在酸中氧化力更强,能氧化负价态的氯、溴、碘、硫等离子及二氧化硫等。与皮肤接触可腐蚀皮肤产生棕色染色,数日不褪(可以使用维生素C或草酸溶液洗去);粉末散布于空气中有强烈刺激性,可使人连打喷嚏。与活泼金属粉末混合后可能會强烈燃烧,危险。在中性溶液中还原产物一般为二氧化锰。另外,该物质的溶液在碱中不稳定,容易生成墨绿色锰酸钾(K₂MnO₄),加入酸又能生成高锰酸钾。
用途
顯色劑
在實驗室常作為顯色劑,用於薄層層析顯色。
淨化空氣
一些空氣清淨機會有CPZ濾網,用來吸收有害氣體。
滴定
維生素C水溶液能將過錳酸鉀溶液褪色,維生素C溶液越濃,用量就越少。根據這特性,就能夠用高锰酸钾測定蔬菜或水果中的維生素含量。
此外,在分析化学中,高锰酸钾还能用来滴定一些还原劑来测定其含量。
工业生产
在化学工业用于生产维生素C、糖精等。在轻化工业中用作纤维、油脂的漂白和脱色。
消毒杀菌
高锰酸钾有强氧化力,其溶液用于消毒杀菌。
储存
高锰酸钾应避光、干燥保存。
其溶液不稳定,缓慢分解并放出氧气。在酸或碱中更不稳定。
参考资料
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||








