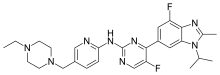
阿貝西利
 | |
| 臨床資料 | |
|---|---|
| 读音 |
/ʌˌbɛməˈsaɪklɪb/ u-BEM-ə-SY-klib |
| 商品名 | 捷癌寧(Verzenio)、Verzenios、Ramiven、Zenlistik |
| 其他名稱 | LY2835219 |
| AHFS/Drugs.com | 消费者药物信息 |
| 核准狀況 | |
| 给药途径 | 口服藥錠 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 |
|
| 藥物動力學數據 | |
| 生物利用度 | 45% |
| 血漿蛋白結合率 | 96.3% |
| 生物半衰期 | 18.3 hrs |
| 排泄途徑 | 81% 經由糞便, 3% 經由尿液 |
| 识别信息 | |
| |
| CAS号 | 1231929-97-7 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| PDB配體ID | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard |
100.233.787 |
| 化学信息 | |
| 化学式 | C27H32F2N8 |
| 摩尔质量 | 506.61 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
阿貝西利(Abemaciclib)是一种用于治疗晚期或转移性乳癌的药物。為礼来公司(Eli Lily)研發的一種CDK4和CDK6选择性抑制剂。
2015年10月,美国食品和药物管理局(FDA)以突破創新治療的名義核准該藥物。2017年9月28日,它被 FDA 批准在美国用于治疗某些乳癌病人。
適應症
2017 年 9 月,此藥物在美國被批准用於“雌激素受體 (HR) 陽性、人類上皮生長因子受體 2 (HER2) 陰性的晚期乳癌病人,或是接受過針對激素的治療後仍病情惡化的轉移乳癌病人。
對乳癌病人的研究,比較以fulvestrant加上安慰劑,以及使用fulvestrant併用abemaciclib的治療,併用abemaciclib的病人無惡化存活期平均為16.4個月,安慰劑組為9.3個月。
副作用
在研究中, 發生率在20%以上的副作用有腹泻、恶心和呕吐、白血球低下(低白血球计数),包括嗜中性白血球低下、贫血、血小板低下、胃痛、感染、疲劳、食欲下降和头痛。
藥物交互作用
由于 abemaciclib 主要由肝臟酵素CYP3A4代谢,因此抑制CYP3A4的藥物(如酮康唑)可能會增加其血浆濃度。反之,CYP3A4 的誘導劑會降低 abemaciclib 的血浆浓度,如利福平。
药理學
作用机制
与同類药物palbociclib和瑞博西利(ribociclib)一樣,abemaciclib 抑制细胞周期蛋白依赖性激酶 4 (CDK4) 和细胞周期蛋白依赖性激酶 6 (CDK6)。这些酶负责磷酸化,可使视网膜母细胞瘤蛋白失活(该蛋白作用於細胞週期從 G1期進展到 S期)。阻断该路徑可防止细胞进入 S 期,从而诱导细胞凋亡。使用癌細胞進行體外研究,發現 abemaciclib 誘導非細胞凋亡性的細胞死亡,特徵是形成了源自溶酶體的細胞質液泡。此結果顯示除了抑制細胞週期蛋白依賴性激酶外,可能還有其他作用機制。
药物动力学

口服后,绝对生物利用度为 45%。平均 8 小时后达到最高血浆浓度(范围:4.1-24.0 小时)。在循环中,96.3% 的 abemaciclib 与血浆蛋白結合。本藥物主要通过肝臟的酵素 CYP3A4 代谢为N-去乙基 abemaciclib (M2),另有較小部分代謝成羟基衍生物 (M18、M20) 和另一种氧化代谢物 (M1)。这些代谢物具有与原藥物相似的高血浆蛋白结合率。
Abemaciclib 主要通过粪便排泄 (81%),少量通过尿液排泄 (3%)。其排除半衰期平均为 18.3 小时。
临床试验
治療乳癌的研究,于 2014 年 5 月和 12 月宣布了成功的 I 期和 II 期試驗結果。
截至2016年初,abemaciclib進行了三個第三期臨床試驗。
- MONARCH 2:研究併用abemaciclib與fulvestrant治療女性乳癌病人,2017 年 3 月,礼来宣布在雌激素受體陽性與和HER2阴性晚期或转移性乳癌,併用組與使用fulvestrant加上安慰劑的對照組相比,無惡化存活期較優。由此,2017 年 9 月 FDA 批准使用。
- MONARCH 3 研究。
化学
可利用鈴木反應以四步驟合成,下一步是Buchwald-Hartwig 胺化,最后一步是使用劉卡特反应的还原胺化。
参考
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
