
B细胞
| B细胞 | |
|---|---|
 电子显微镜下的人类B细胞
| |
| |
| 基本信息 | |
| 系統 | 免疫系统 |
| 标识字符 | |
| 拉丁文 | lymphocytus B |
| MeSH | D001402 |
| FMA | FMA:62869 |
| 《显微解剖学术语》 | |
B细胞(英語:B cell),也称B淋巴球(B lymphocyte),是白血球中一種淋巴細胞的亞型。B細胞屬於後天免疫系統的體液免疫,作用為分泌抗體。此外,B細胞能呈現抗原(也屬於抗原呈遞細胞)並分泌細胞激素。哺乳動物的B細胞在骨髓中成熟,骨髓位於多數骨骼的核心。鳥類的B細胞在腔上囊(Bursa of Fabricius)中成熟,腔上囊是一種淋巴器官,「B」其實是指腔上囊,而不是一般認為的骨髓(Bone marrow)。
发育
它来源于骨髓中的造血干细胞,在骨髓中成熟,在體液免疫中產生抗體,起到重要作用。當遇到抗原時,會分化成核比例較大的漿細胞。漿細胞的細胞質中且會出現一些顆粒,這些顆粒容易被甲基藍等天青染料所染色,同時會出現抗體,表現在細胞膜或釋放出去。另一部分B细胞经过抗原激活后并不成为浆细胞,而是成为记忆B细胞。当再次遇到相同抗原时,记忆B细胞能迅速作出反应,大量分化增殖。
B细胞在骨髓中需要经过两轮筛选才能够发育为正常的B细胞。第一轮阳性选择与抗原反应无关,是针对B细胞受体(BCR)以及其前体pre-BCR的。如果这些受体不能很好地结合它们的配体,B细胞就会停止发育。第二轮阴性选择则是检查B细胞与自身抗原的结合力,如果结合力过强,B细胞就会凋亡。阴性选择确保了免疫耐受的状态,使得B细胞不会对自体抗原发生免疫反应。
为了完成发育,非成熟B细胞需要从骨髓迁移到脾脏,完成过渡期。B细胞的过渡期分为T1和T2期。从B细胞离开骨髓到它们迁入脾脏,这段时间的B细胞属于T1期B细胞。而T1期B细胞将在脾脏中发育为T2期B细胞。取决于它们通过BCR和其他受体接收到的信号,T2期B细胞既可以分化为滤泡(FO)B细胞,也可以分化为边缘区(MZ)B细胞。一旦分化完成,它们就被视为成熟(mature)B细胞,或者说初级(naive)B细胞。
活化
B细胞活化发生在次级淋巴器官,例如脾脏和淋巴结。在B细胞离开骨髓,随着血流迁移到次级淋巴器官的过程中,会始终接收来自淋巴循环的抗原。在次级淋巴器官内,当B细胞通过BCR结合抗原时,B细胞活化就开始了。虽然B细胞活化的详细机理尚未解明,但是有观点认为其符合类似T细胞活化的动力学模型。即在静息状态下细胞膜上的BCR处于磷酸化和去磷酸化的平衡中,而B细胞与抗原呈递细胞的接触将使平衡往BCR磷酸化的方向倾斜,从而起始B细胞的活化。在3类B细胞中,滤泡B细胞更倾向于发生依赖T细胞的活化,而边缘区B细胞和B1细胞更倾向于发生不依赖T细胞的活化。
细胞表面受体CD21、CD19和CD81可以组成B细胞共受体复合物,而CD21的表达可以增强B细胞的活化。 当BCR结合了一个与C3补体蛋白片段的抗原时,CD21可以与C3补体结合,激活CD19和CD81的下游信号,从而使细胞更容易被活化。
依赖T细胞的活化
包括蛋白质抗原的一部分抗原,必须依赖T细胞才能活化B细胞,这类抗原称为T细胞依赖(TD)抗原。这类抗原无法在缺少T细胞的机体内引发体液免疫反应。这类抗原引发的免疫反应往往需要几天时间,产生的抗体相对于不依赖T细胞的反应,亲和力更高,功能也更广泛。
TD抗原和BCR结合后,就会被B细胞胞吞进入细胞内。这些抗原被切割为片段后,以和MHC-II分子结合的状态回到细胞膜上。辅助T(TH)细胞,特别是滤泡辅助T(TFH)细胞,将会以自身的T细胞受体(TCR)识别B细胞表面结合了抗原片段的MHC-II分子。TCR成功识别结合MHC-II分子后,T细胞将在细胞表面表达CD40L蛋白质,并分泌白血球介素-4和白血球介素-21等細胞激素。CD40L和B细胞表面CD40分子的结合对B细胞活化是必要的。这一过程将促进B细胞增殖、免疫球蛋白类型转换、體細胞超突變、以及T细胞发育和分化。来自T细胞的细胞因子也发挥类似的作用。一旦B细胞接受了上述来自T细胞的信号,这个B细胞就被认为是活化了。
活化后的B细胞将分化为提供快速保护的短寿命浆母细胞,以及提供长期保护的长寿浆细胞和记忆细胞。分化的第一步发生在淋巴结滤泡外的次级淋巴器官,在这一步分化中,活化B细胞增殖,可能发生免疫球蛋白类型转换,最终分化成浆母细胞,分泌的抗体类型主要是结合力相对较弱的IgM。第二步分化中,活化B细胞将进入淋巴结滤泡并形成生发中心。生发中心是专门适应B细胞增殖分化的微环境,B细胞在其中大量增殖,发生免疫球蛋白类型转换,并在体细胞超突变中完成亲和力成熟。生发中心中的TFH细胞能加速这项工程,并最终产生具有高亲和力和较长寿命的记忆细胞和浆细胞。这些可以分泌大量抗体的浆细胞可能留在次级淋巴器官中,但更有可能会迁移回骨髓。
不依赖T细胞的活化
包括外源多糖和未甲基化CpG DNA在内的T细胞非依赖抗原,即使在缺少T细胞的机体内也可以活化B细胞,引发体液免疫反应。这样的免疫反应相对来说更快速,但是产生的抗体亲和力相对较低,功能也相对局限。
TI抗原也需要一些额外信号来完成对B细胞的活化,这些额外信号可能是B细胞上Toll样受体对常见微生物组分的识别,也可能是细菌表面重复抗原表位造成的B细胞表面BCR广泛交联。被TI抗原活化的B细胞将在滤泡外的次级淋巴器官中增殖,经过可能的免疫球蛋白类型转换,最终分化为提供快速短时防护的浆母细胞,以及一部分长寿浆细胞。
记忆B细胞活化
记忆B细胞在识别到特定抗原后活化,这一抗原的种类在其最初分化时就已决定。一些记忆B细胞不需要T细胞的帮助就可以被活化,例如某些病毒特异性记忆B细胞;但是其他的记忆B细胞仍然需要T细胞的帮助才能活化。和初次免疫反应类似,记忆B细胞的BCR结合特定抗原后,抗原就会被B细胞胞吞加入细胞内。这些抗原被切割为片段后,以和MHC-II分子结合的状态回到细胞膜上。对同一个抗原有记忆的记忆辅助T(TH)细胞,特别是滤泡记忆辅助(TFH)细胞,将会以自身的TCR识别记忆B细胞表面结合了抗原片段的MHC-II分子。相似的,在此之后,经过接受T细胞的信号转导,活化的记忆B细胞将在滤泡外增殖分化为浆母细胞和浆细胞,或者在生发中心内分化成浆细胞和记忆细胞。在第二次免疫反应中,记忆B细胞是否会在生发中心进行进一步的亲和力增强尚不明确。
B细胞分类
- 浆母细胞:一种寿命较短,可增殖,可分泌抗体的B细胞。产生于免疫反应早期,其分泌的抗体相对于浆细胞而言亲和力较低。
- 浆细胞:一种寿命较长,不再增殖,可分泌抗体的B细胞。有证据表明,初级B细胞分化到浆细胞的过渡阶段与浆母细胞类似。相对于浆母细胞,浆细胞由于在生发中心中完成了亲和力成熟过程,分泌的抗体亲和力较高,分泌抗体的量也更多。
- 淋巴浆细胞样细胞:一种具有浆细胞特征的B细胞。这种细胞类型出现于前期或恶性漿細胞惡病質,与IgM的过度分泌相关。
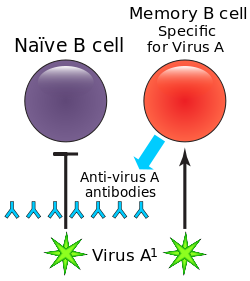
- 记忆B细胞:一种寿命很长,处于休眠期的B细胞。它们在血液中循环,一旦遇到其原来分化来的B细胞曾识别的特定抗原,就可以起始快速而强力的免疫反应。
- B-2细胞:
- 滤泡(FO)B细胞:有时也称为B-2细胞。最常见的一类B细胞,除了在血液中,主要存在于次级淋巴器官的滤泡内。免疫反应中高亲和力的抗体主要是它们的功劳。
- 边缘区(MZ)B细胞:主要在脾脏的边缘区被发现。由于脾脏的边缘区的血流量很高,它们是对抗血源性病原体的第一道防线。相对而言更容易发生不依赖T细胞的B细胞活化。
- B-1细胞:发育途径不同于滤泡B细胞和边缘区B细胞。在小鼠体内,它们主要存在于胸膜腔和腹膜腔,生产天然抗体(在无感染的情况下产生的抗体),抵抗粘膜病原体,主要发生不依赖T细胞的B细胞活化。在人体内尚未找到和小鼠B-1细胞真正同源的细胞群,但是有和B-1细胞类似的细胞群存在。
- 调节B细胞:一类免疫抑制细胞,通过分泌IL-10、IL-35和TGF-β来抑制病理性、促炎症的淋巴细胞扩增。同时,它们也通过影响T细胞的分化,来促进调节T(Treg)细胞的产生。尚未有统一的Breg细胞特征被阐明,但是多种具有类似功能的Breg细胞亚群已在人类和小鼠中被发现。关于这些Breg细胞亚群之间的关系,以及Breg细胞的分化途径,现在仍然有待研究。[25]有证据表明任何类型的B细胞都可能在炎症信号的刺激下分化为Breg细胞。
相关疾病
异常B细胞识别自身抗原,并分泌攻击自身组分的抗体时,可能导致自身免疫病。与B细胞异常相关的自身免疫病包括硬皮病、多发性硬化、系统性红斑狼疮、一型糖尿病和类风湿性关节炎。
B细胞及其前体的恶性转化可以引发癌症,包括B細胞慢性淋巴細胞白血病、急性淋巴性白血病、毛细胞白血病、滤泡性淋巴瘤、非霍奇金淋巴瘤、霍奇金淋巴瘤。浆细胞的恶性病变则包括多发性骨髓瘤、華氏巨球蛋白血症、以及某些形式的淀粉样变性。
参见
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
